【前沿进展】巨噬细胞装备升级,CAR-M正式进军实体瘤治疗战场
截至2021年5月,全球已有近1300多项关于CAR-T的临床试验证明了CAR-T细胞疗法在癌症治疗特别是血液肿瘤治疗中的巨大优势,然而其对实体瘤的治疗效果却十分有限。不同于血液瘤,实体瘤能够构建具有免疫抑制特性的肿瘤微环境(tumor microenvironment, TME),从而影响CAR-T疗法的功效。TME免疫抑制性改变会阻止免疫细胞向病灶的运输及T淋巴细胞对肿瘤的浸润,少数能够浸润实体瘤的T细胞免疫反应仍可能受到微环境中免疫抑制细胞或抑制因子的限制。此外,实体瘤的高度异质性也限制了靶向单一抗原的CAR-T疗法的疗效。
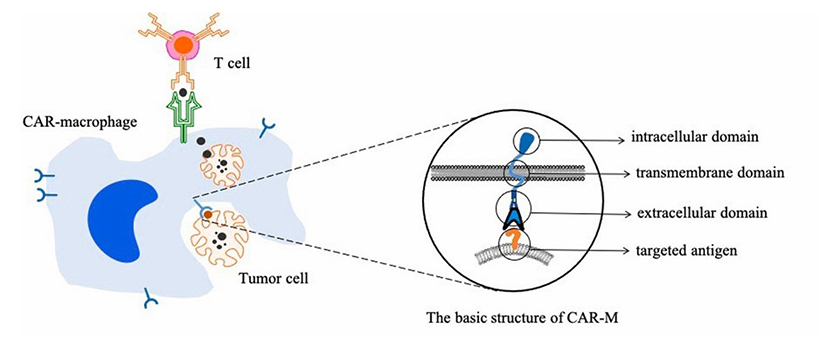
基于CAR-T细胞疗法在临床应用中的优势,研究人员尝试并成功改造其他工程化CAR免疫细胞,试图克服CAR-T治疗的局限性,为实体瘤治疗提供新的方向。其中,CAR修饰的巨噬细胞(CAR-M)被认为是一种有前途的细胞类型。巨噬细胞主要通过吞噬体液和组织中的细胞残片及病原体并呈递抗原以激活淋巴或其他免疫细胞,令其对病原体做出反应。在肿瘤微环境中,巨噬细胞是具有最高浸润率的先天免疫细胞并可与TME中几乎所有细胞成分相互作用,刺激血管生成,增加肿瘤浸润,并介导免疫抑制(1)。
肿瘤相关巨噬细胞(tumor-associated macrophage, TAM)同时具有肿瘤杀伤作用及促肿瘤作用。M1 型巨噬细胞被TLR或Th1细胞因子激活,具有很高的抗原呈递能力的同时,还分泌活性氧(ROS)及促炎性细胞因子,与癌症良好预后相关。相反,M2样巨噬细胞被Th2衍生的细胞因子极化,促进组织修复。同时,M2样巨噬细胞可通过分泌肾上腺髓质素和血管上皮生长因子(VEGF)支持血管生成并表达免疫抑制分子,从而促进肿瘤生长(4) (图2)。
不同于T细胞,巨噬细胞是身体对病毒感染的第一反应者,因此被认为是细胞治疗的重要方向。然而,由于巨噬细胞不易被基因疗法和细胞疗法中使用的标准病毒载体转染,导致通过基因改造细胞攻击癌症的尝试止步不前。2021年3月18日,美国Carisma Therapeutics公司(以下简称为Carisma),宣布完成首例靶向Her2的CAR-M 疗法(CT-0508)受试者给药,标志着CAR-M改造治疗实体瘤进入新纪元& lt;/span>(6)(相关科研进展免费下载)。
M1/M2表现型极化,助力CAR-M 细胞疗法开发,帮助您缩短研发周期。
生物素标记蛋白
| 分子 | 货号 | 产品描述 |
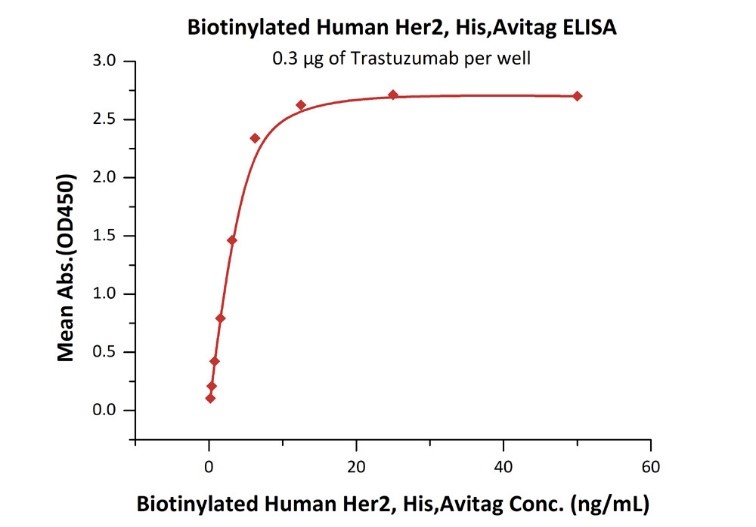
| Biotinylated Human Her2 / ErbB2 Protein, His,Avitag™ | ||
| | ||
| | ||
| | ||
| | | |
| | ||
| | ||
| |
点击图表中分子或产品内容可查看详细信息
| 分子 | 货号 | 产品描述 |
| | ||
| | ||
| | ||
| | ||
| | ||
| | ||
| | ||
| |
活性(Bioactivity)-FACS
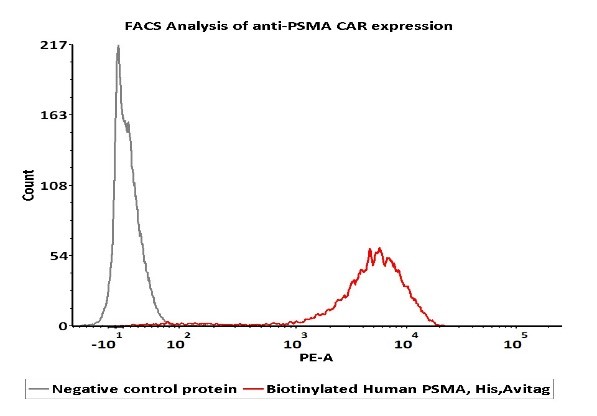
2e5 of PSMA-CAR-293 cells transfected with anti-PSMA-scFv were stained with 100μl of 1μg/mL of Biotinylated Human PSMA, His,Avitag (Cat. No. PSA-H82Qb) and negative control protein respectively, washed and then followed by PE-SA and analyzed with FACS (Routiney tested).
快来下载免费资料包,
了解更多CAR-M最新科研进展详细信息~
您可通过以下方式联系到ACROBiosystems:
邮件:inquiry@acrobiosystems.com
电话:15117918562
微信:扫描下方二维码即可进行沟通

(请备注公司+姓名)
参考文献:
1. Chen Y, Yu Z,Tan X, Jiang H, Xu Z, Fang Y, et al. CAR-macrophage: A newimmunotherapy candidate against solid tumors. Biomed Pharmacother.2021;139:111605.
2. Mangal JL, Handlos JL,Esrafili A, Inamdar S, McMillian S, Wankhede M, et al. Engineering Metabolismof Chimeric Antigen Receptor (CAR) Cells for Developing EfficientImmunotherapies. Cancers (Basel). 2021;13(5).
3. Morrissey MA, WilliamsonAP, Steinbach AM, Roberts EW, Kern N, Headley MB, et al. Chimeric antigenreceptors that trigger phagocytosis. Elife. 2018;7.
4. Jayasingam SD, CitartanM, Thang TH, Mat Zin AA, Ang KC, Ch\'ng ES. Evaluating the Polarization ofTumor-Associated Macrophages Into M1 and M2 Phenotypes in Human Cancer Tissue:Technicalities and Challenges in Routine Clinical Practice. Front Oncol.2019;9:1512.
5. Klichinsky M, Ruella M,Shestova O, Lu XM, Best A, Zeeman M, et al. Human chimeric antigen receptormacrophages for cancer immunotherapy. Nat Biotechnol. 2020;38(8):947-53.
6. http://www.globecancer.com/azzx/show.php?itemid=12109